文章来源 光影 生物医学科研之家 昨天
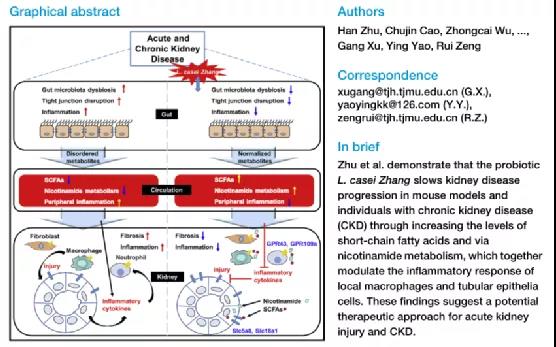
累积的证据表明,肠道微生物群的不平衡,被称为生态失调,而肠道黏膜屏障的损害与炎症、氧化应激和各种肾脏疾病的肾损伤有关,包括糖尿病肾病、狼疮肾炎和IgA肾病。此外,异常的肠道微生物群会改变宿主的代谢组学,并对各种肾脏疾病的结果产生负面影响,特别是慢性肾脏疾病 (CKD)。事实上,由于肠道微生物群不断与宿主的重要器官相互作用,如肾脏、大脑和骨髓,肠道-肾脏轴理论已经被提出。该理论认为,胃肠道或肾脏的任何变化可能通过多种途径相互影响,包括能量代谢、蛋白炎性免疫反应、肠道黏膜和肠道菌群。这种肠肾相互作用的结果是相互因果关系,识别急性肾损伤 (AKI)和CKD的病理生理机制已成为近年来研究的热点。然而,肠道菌群的变化如何影响肾脏疾病的进展仍有待阐明。

2021年7月8日,来自中国武汉华中科技大学同济医学院肾内科的Rui Zeng及其团队在Cell Metab (IF: 21.567)杂志上发表名为The probiotic L. casei Zhang slows the progression of acute and chronic kidney disease的研究[1]。
研究亮点
干酪乳杆菌改善急性肾损伤和慢性肾病小鼠模型的肾功能和病理学。
干酪乳杆菌改善急性肾损伤和慢性肾病患者的肠道微生物菌群失调。
干酪乳杆菌通过SCFAs和烟酰胺减少肾脏炎症和损伤。
干酪乳杆菌减缓3-5期慢性肾病患者的肾功能衰退。
主要结果
口服干酪乳杆菌减轻I/R诱导的损伤后的AKI和随后的慢性肾纤维化
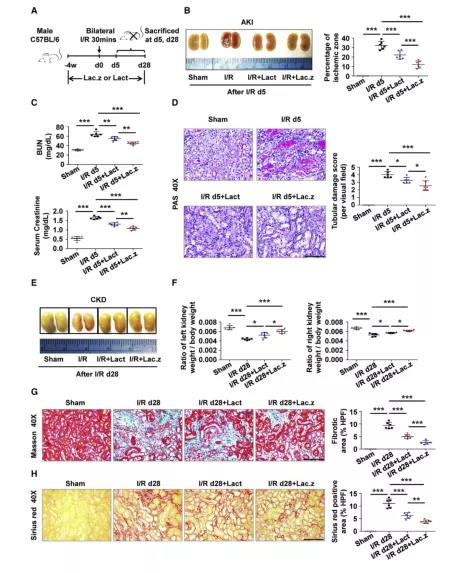
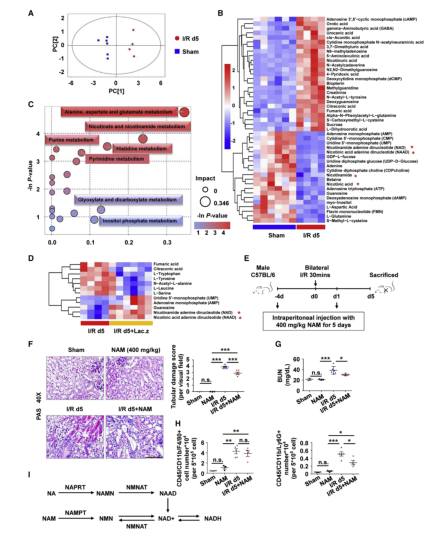
为探讨干酪乳杆菌对肾损伤的影响,我们分别对雄性C57BL/6小鼠灌胃或不灌胃干酪乳杆菌。在受到I/R诱导的损伤之前,将干酪乳杆菌 (Lac.z)或嗜酸乳杆菌 (Lact)培养4周 (图1A)。在损伤后第5天处死小鼠时,在损伤肾脏的皮质和髓质交界处观察到一个易于观察到的缺血区。然而,与未治疗组相比,益生菌预处理组的损伤程度明显较小,Lac.z预处理比Lact预处理更有效 (图1B)。此外,与I/R组相比,益生菌预处理不仅降低了血清尿素氮 (BUN)和肌酐 (肾功能改善的指征),还降低了坏死、肾小管扩张、管型形成和刷状边缘缺失等病理损伤 (图1C和1D)。
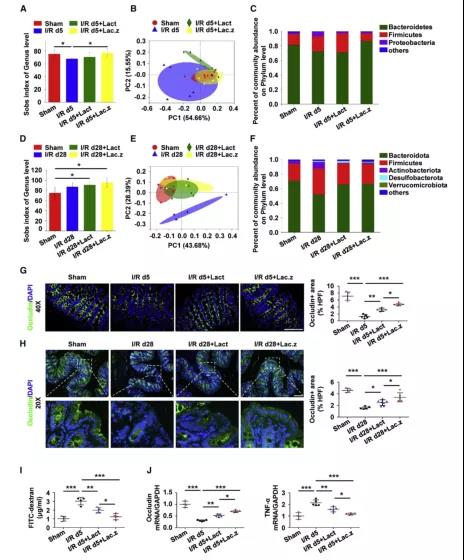
干酪乳杆菌预处理可改善I/R诱导的肠道微生物失调
I/R诱导损伤后第5天 (作为AKI模型)和第28天 (作为CKD模型),通过粪便16S rRNA基因测序分析检测肠道微生物菌群失调。我们使用Sobs指数分析了α多样性,在第5天,I/R组的α多样性指数显著低于假手术组。然而,我们发现Lac.z预处理导致I/R后的Sobs多样性指数显著高于未处理组,与假手术组相似,而Lact预处理与未处理组无差异 (图2A)。
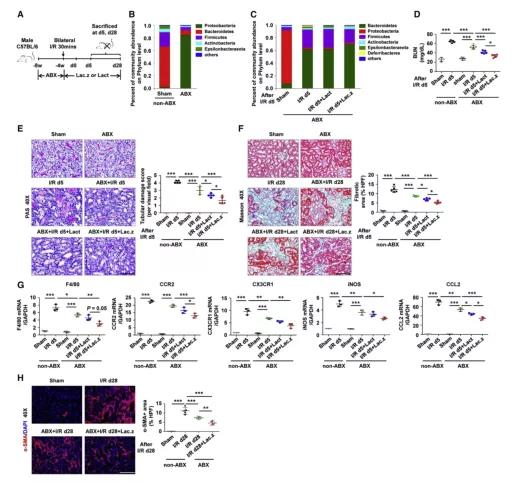
干酪乳杆菌提供的肾脏保护作用并不完全依赖于原始肠道菌群
为了研究肠道菌群在肾损伤中的作用以及益生菌治疗的效果是否依赖于原始肠道菌群,我们使用广谱抗生素 (ABX)耗竭原始肠道菌群4周,然后在开始I/R诱导的损伤之前再进行4周的口服益生菌治疗预处理 (图3A)。我们发现,肠道菌群组成在门水平上的变化与之前在未接受ABX治疗但接受益生菌预处理的小鼠中的发现一致;即拟杆菌组较大,厚壁菌属较低 (图3B和3C)。此外,我们发现,通过ABX用法消耗肠道菌群后,即使两组均未接受益生菌预处理,I/R后第5天与未接受ABX治疗的小鼠相比,肾损伤程度较轻 (图3D和3E)。
我们采用UHPLC-MRM-MS/MS分析技术检测儿童组中其他代谢产物的变化,共检测到149种化合物。从OPLS-达评分图中,我们发现假手术组和I/R d5组之间的代谢产物有显著差异 (图5A)。分层聚类分析热图显示两组主要差异代谢产物 (图5B),通过代谢途径分析发现,I/R d5组烟酰胺代谢 (包括NAD和NAAD)显著降低 (图5C),而干酪乳杆菌预处理导致烟酰胺含量高于未处理对照组 (图5D)。
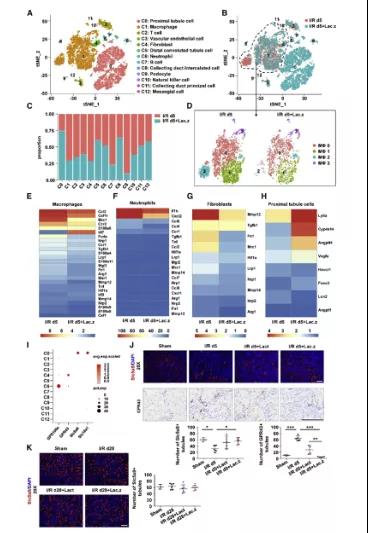
酪乳杆菌的保护作用依赖于免疫调节巨噬细胞和肾脏TECs
干酪乳杆菌诱导的肾保护,我们对I/R后第5天从经干酪乳杆菌预处理的小鼠解剖的肾样本以及未处理对照的样本进行单细胞RNA测序 (scRNA-seq),并鉴定出13个细胞簇 (图6A)。与非治疗组相比,我们发现干酪乳杆菌预处理组中巨噬细胞显著减少,这与我们通过流式细胞术和免疫染色获得的结果一致。差异分析确定,与非治疗组相比,经干酪乳杆菌预处理后,I/R后第5天来自近端小管的巨噬细胞明显减少且细胞保存更好 (图6B和6C)。
结论及展望
在本研究中,我们确定了肠道菌群失调和益生菌在肾脏疾病进展中的作用。我们描述了肠道菌群失调是介导肾炎症和进行性纤维化的关键事件。与嗜酸乳杆菌相比,干酪乳杆菌能够更好地改善肠黏膜屏障功能,并通过有益代谢产物 (尤其是SCFAs和烟酰胺)抑制炎性信号扩张。这些代谢产物显著抑制巨噬细胞诱导的对AKI后renalTECs的促炎反应,同时延缓CKD的后续发展。然后,我们进行了一项体内依赖性人类研究,以调查干酪乳杆菌的效用是否会影响3-5期CKD患者的肾脏疾病进展。我们发现,CKD患者的肠道菌群稳态受损,给予干酪乳杆菌安全且有益。此外,基于小鼠研究,我们得出结论,干酪乳杆菌通过肠道微生物群来源的代谢产物有益地影响免疫调节性巨噬细胞的调节和肾TEC的炎性反应,从而预防AKI并减缓CKD的进展。
原文链接
https://www.sciencedirect.com/science/article/pii/S1550413121002849?via%3Dihub
参考文献
1.Zhu Han,Cao Chujin,Wu Zhongcai et al. The probiotic L. casei Zhang slows the progression of acute and chronic kidney disease.[J] .Cell Metab, 2021, undefined: undefined.