引自 蕾玖 生物医学科研之家
 图
图
导读
生命早期的免疫-微生物相互作用影响着过敏、哮喘和其他炎症性疾病的风险。母乳喂养通过为专门的微生物提供营养物质,引导健康的免疫-微生物关系,而这些微生物反过来又有利于宿主的免疫系统。作者表明,缺乏双歧杆菌,与生命早期的系统性炎症和免疫失调有关。补充婴儿双歧杆菌EVC001,降低肠道Th2和Th17细胞因子上调IFNβ,双歧杆菌所表达的HMOs利用基因激活代谢通路,增加了吲哚-3-乳酸,衍生的吲哚-3-乳酸在极化过程中上调了Th2和Th17细胞的免疫调节性半乳糖凝集素-1,维护了新生儿最初几个月的有益微生物和免疫调节之间的稳定性。题目:Bifidobacteria-mediated immune system imprinting early in lifeDOI:https://doi.org/10.1016/j.cell.2021.05.030①在微生物的相互作用下,婴儿出生后存在有序的免疫普变化规律。②肠道双歧杆菌所表达的HMO利用基因的缺乏,会引起生命早起的系统性炎症。③补充婴儿双歧杆菌EVC001,降低肠道Th2和Th17细胞因子上调IFNβ。④EVC001相关的吲哚-3-乳酸可上调T细胞中的抑制性半乳糖蛋白-1。
 图
图
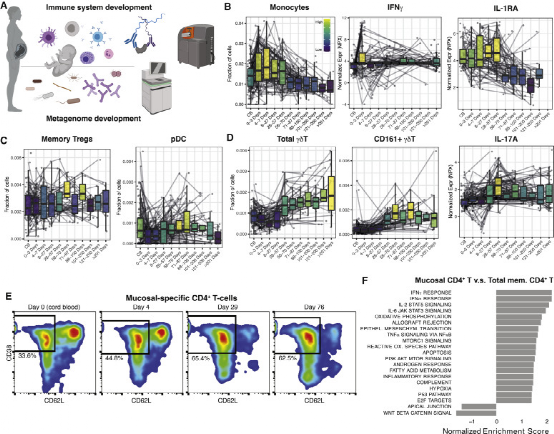
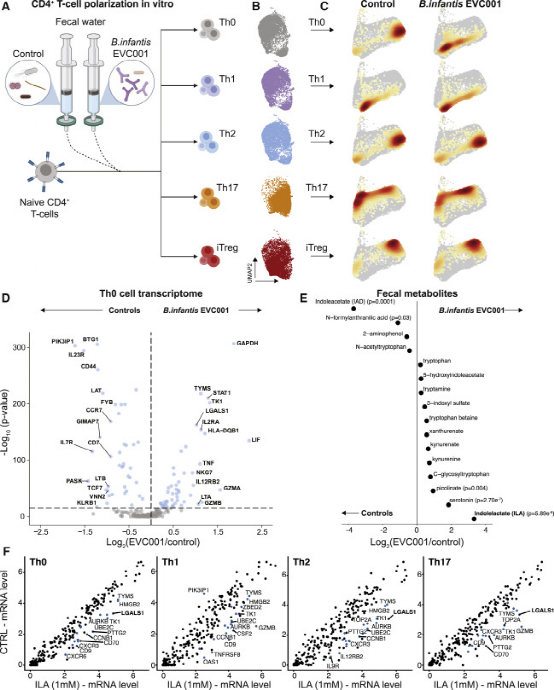
生命早期的免疫-微生物相互作用会影响到以后的免疫介导疾病的风险;然而,确切的机制仍然难以捉摸。本文的结果扩展了作者以前对由微生物定植引发的免疫学事件序列的理解,这导致平衡的免疫微生物关系或不同程度的肠道和全身炎症以及扰乱免疫细胞调节。作者发现在 T 细胞区中,双歧杆菌种类的低丰度和/或 HMO 使用能力的缺乏与异常 Th2 和 Th17 反应驱动的肠道炎症有关。婴幼儿双歧杆菌EVC001是一种双歧杆菌菌株,具有分解所有HMO糖苷键的全部遗传能力,在体外使新生T细胞向Th1极化,而未被婴幼儿双歧杆菌EVC001定植的婴儿的粪水则使Th2和Th17类型的细胞极化。在生命早期,新产生的幼稚T细胞填充粘膜组织并分化成记忆T细胞,这表明微生物群影响粘膜免疫的机会窗口。
 图
图
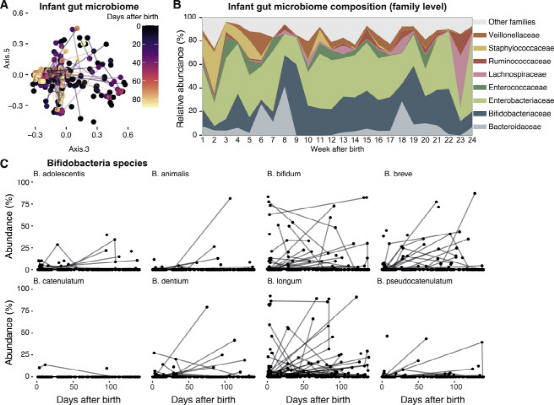
来自小鼠数据的流行理论假设对定植微生物的定时反应通过诱导耐受性在肠道中建立健康的免疫微生物界面。这里描述的短暂的免疫细胞激活事件让人联想到小鼠对定植微生物的这种短暂的 "断奶反应",但人类新生儿的时间明显不同,而且这种反应与断奶无关。作者队列中的大多数婴儿的母乳喂养时间超过了3个月的窗口期,在此期间似乎会发生最引人注目的免疫细胞反应。此外,在人类新生儿中看到的反应类型在质量上是不同的,与在小鼠中看到的变化相比,涉及不同的细胞群,这不仅仅是由于人类的血液分析和小鼠的肠道分析之间的差异。
 图
图
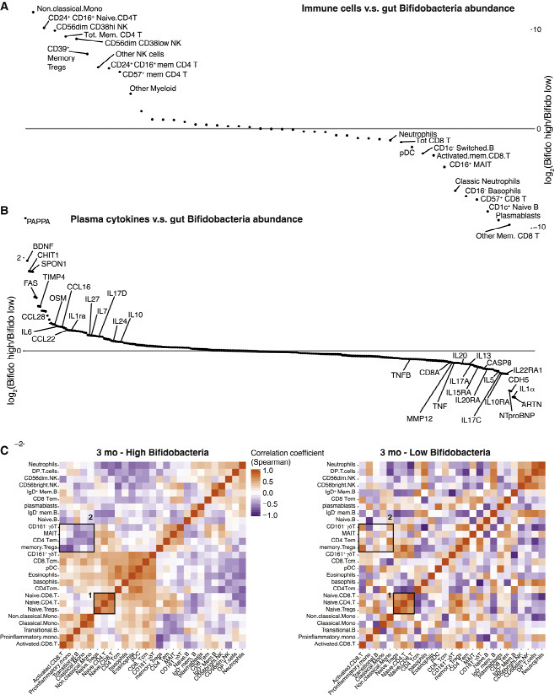
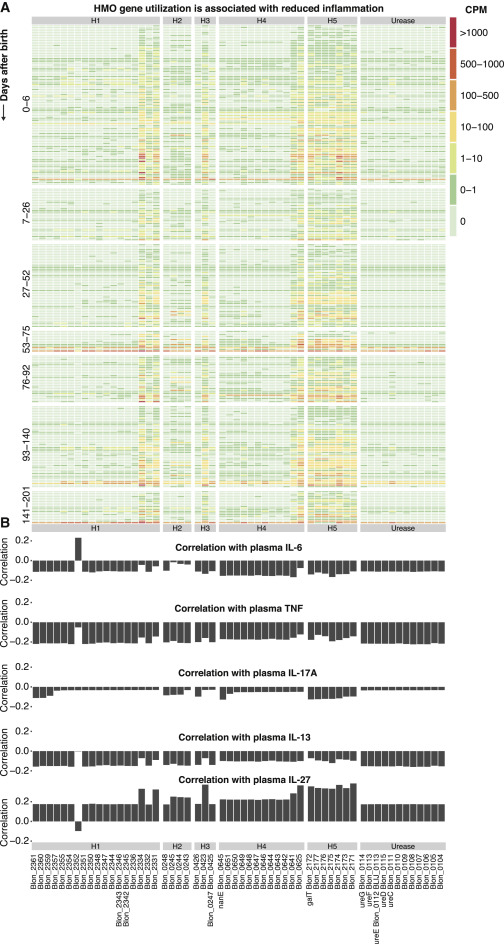
微生物群的耐受性诱导是防止组织损伤和炎症的关键,作者的研究表明如何在人类婴儿中诱导这种耐受性。作者发现,能够代谢HMOs的双歧杆菌与促炎症标志物的减少有关,相反,IL-10和IL-27等蛋白的升高与调节性T细胞有关。另外,在双歧杆菌丰富的儿童中,记忆性Treg频率与促炎症单核细胞丰度和活化T细胞群丰度成反比,这种调节关系在缺乏这种有益微生物的儿童中消失。已知定植有双歧杆菌的婴儿会产生高水平的短链脂肪酸,而这些是肠道内调节性T细胞的重要诱导剂。此外,作者发现了一个额外的可能的耐受性诱导剂,即肠道IFNβ,与未被婴儿病菌定植的婴儿相比,在补充婴儿病菌EVC001的婴儿中产生的浓度明显更高。这一发现与最近的研究结果一致,该研究表明特定的双歧杆菌通过诱导小鼠结肠DCs产生IFNβ来维持病毒感染期间的宿主健康。另外,其他研究也描述了微生物诱导的IFNβ在决定对病毒挑战的免疫反应中的作用。多发性硬化症患者的IFNβ治疗可诱导调节性T细胞产生IL-10,小鼠的IFNβ可诱导调节性T细胞,这些都表明,由定植的有益微生物直接或间接诱导的肠道IFNβ产生是确保肠道耐受性的另一种机制。
 图
图
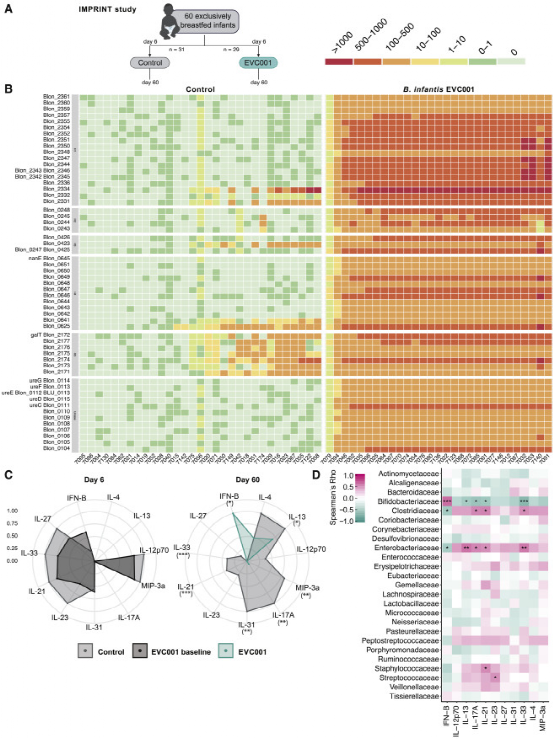
尽管在所研究的两个队列中都检测不到婴儿肠道杆菌EVC001菌株,但对HMO利用基因的关注使作者能够对这些儿童进行直接比较。重要的是,与HMO利用基因丰度有关的免疫系统状态的相似性是对作者发现的独立确认。这表明对发育中的婴儿免疫系统的印记效应并不依赖于特定的微生物菌株,而是依赖于元基因组的核心功能特性,如代谢HMO的能力和产生关键的下游代谢物,如ILA。
 图
图
有机酸、乙酸盐和丙酸盐先前已参与到缓解动物模型的肺部炎症和人类婴儿的食物过敏。在母乳喂养的婴儿中产生的ILA,虽然没有解决免疫系统的变化,但已被证明可以通过激活AhR和Nrf-2减少肠道炎症。进一步支持双歧杆菌衍生的ILA作用的是最近的一份研究,显示在LPS刺激下通过AhR和HCAR3诱导CD4+T细胞产生IL-22和调节单核细胞TNFα反应。作者的数据与这项研究一致,但增加了更多的免疫学细节,如ILA介导的对Th2和Th17细胞的直接影响,以及负调节器半乳糖凝集素-1的上调。这一发现与乳糜泻患者的数据相比也很有趣,其中半乳糖凝集素-1的大量上调已被证明能诱导耐受性肠道反应。作者认为,这种在生命早期确保肠道耐受性的机制,应该进一步研究,并在随后的临床试验中测试其治疗潜力。
 图
图
重要的是,双歧杆菌物种在利用HMOs的能力上有所不同。具体来说,运输HMOs所需的所有蛋白质和分解HMOs中糖苷键所需的酶仅在长叶双歧杆菌亚种的一些成员中保守,其中婴儿肠道菌的HMO利用位点已被确定,尽管不同婴儿肠道菌株之间HMO分解代谢的差异最近才被确定,这影响了它们在婴儿肠道的生态适应性。作者的数据阐明了微生物组获取和代谢HMOs的总体能力与粘膜和系统性炎症水平下降之间的联系。总的来说,这些数据为有益微生物在生命早期免疫系统印记过程中的作用提供了额外的细节,并为以前报道的相关数据提出了可能的解释,这些数据显示生命早期定植于双歧杆菌物种的婴儿不太可能发生免疫介导的疾病。此外,这些结果强调了在免疫学发展的关键窗口期进行早期微生物群定植的重要性,在这个窗口期存在着补充婴儿肠道微生物群的机会,对幼儿在生命早期和长期都有潜在的好处。